
Evogliptina é um inibidor de DPP4 desenvolvido ao longo de 10 anos de pesquisa pela empresa farmacêutica sul-coreana Dong-A. Aprovada pela agência regulatória da Coreia do Sul para tratamento de diabetes tipo 2 desde 2015, a evogliptina encontra-se em comercialização na Coreia do Sul desde 2016.
Eurofarma conduziu estudo clínico junto à população brasileira e possui parceria para registrar, fabricar e comercializar o produto no Brasil e na América Latina.
Princípio ativo: Tartarato de evogliptina
Classe terapêutica: Inibidor de DPP4
Apresentação: Comprimido revestido 5 mg; Embalagens com 30 comprimidos revestidos
USO ORAL - USO ADULTO
Indicação: Indicado como adjuvante à dieta e exercício para melhorar o controle glicêmico em pacientes com diabetes mellitus tipo 2 em monoterapia ou terapia combinada.

O tartarato de evogliptina (evogliptina) é um novo inibidor de DPP4 desenvolvido para o tratamento da diabetes mellitus tipo 2 por via oral1,9.
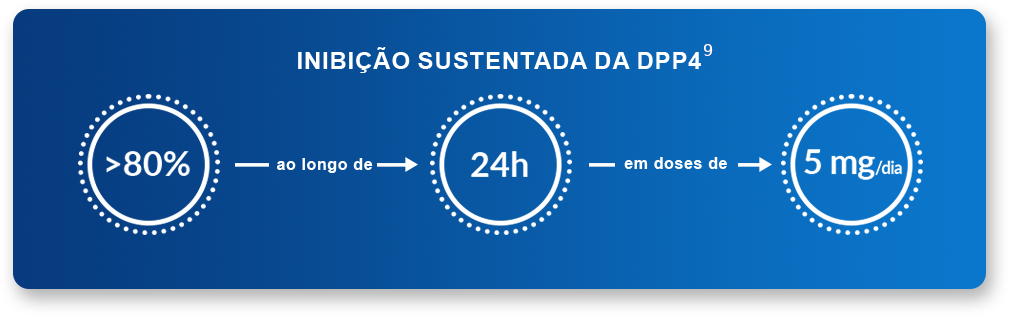
Os estudos realizados com evogliptina corroboram a indicação pretendida: inibição potente e seletiva da enzima DPP4 superior a 80% após administração oral uma vez ao dia em pacientes diabéticos tipo 2 sem necessidade de ajuste de dose em pacientes portadores de insuficiência renal e/ou hepática moderadas, com baixo potencial de hipoglicemias e de interações medicamentosas11-13.
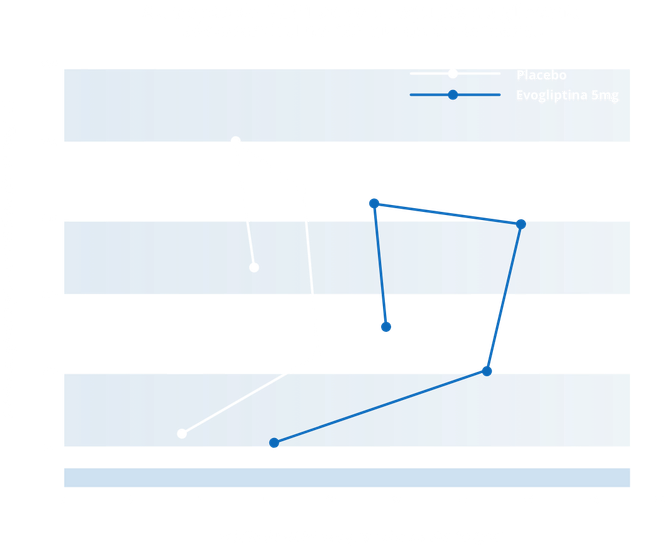
Fig. 6: Aumento de GLP1 ativo e modificação de glicemia pós-prandial no 10° dia de tratamento com placebo (preto) e evogliptina 5 mg 1x/dia (vermelho). Eixo x : média de glicose pós-prandial (mg/dl). Eixo y: média de GLP-1 (pM). Avaliações realizadas 0; 0,25; 0,5; 1 e 2 horas após alimentação. Adaptada de: Gu N, et al. Drug Des Devel Ther. 2014 Oct 6;8:1709-218
Sabe-se que a enzima DPP4 compartilha especificidade de substrato com DPP8, DPP9 e FAP, além disso, o modo de ligação dos inibidores de DPP4 ao sítio catalítico da enzima DPP4 pode aumentar não apenas sua atividade inibitória, mas também sua seletividade contra outras prolil peptidases relacionadas14-16. Estudos anteriores sugeriram que a inibição de DPP8 e DPP9 pode causar respostas tóxicas, incluindo alopecia, trombocitopenia, anemia15. A evogliptina demonstrou excelente eficácia e seletividade na inibição da DPP4 com baixa potência inibitória da DPP8 e da DPP912,13.


Evogliptina apresenta farmacocinética linear e a principal rota de eliminação em humanos é não-renal8,13. A fração de evogliptina excretada inalterada na urina é de 17% a 34% da dose administrada, e a taxa de depuração renal é aproximadamente 30% da depuração aparente total em humanos8,13
A etiologia da doença renal crônica (DRC) é variável e inclui diabetes mellitus, uso de substâncias nefrotóxicas, doenças autoimunes, dentre outras. Além disso, é importante ressaltar que os pacientes portadores de DRC também podem ter doenças associadas, como hipertensão e DM2, necessitando de cuidados mais frequentes de diferentes profissionais de saúde, cujas prescrições podem colocá-los em risco de eventos adversos e segurança como resultado de muitos fatores, incluindo erros de dosagem de medicamentos e uso de drogas nefrotóxicas, que podem causar declínio da função renal. No caso particular dos pacientes portadores de DRC e DM2, a ocorrência de hipoglicemias, frequentemente associadas a algumas classes de antiabéticos e eventualmente com potencial risco morte é um fator determinante para escolha de medicações de primeira linha, bem como associações de medicações para controle glicêmico20,21.
Devido à boa tolerabilidade e ao baixo risco de promover hipoglicemia inerente ao mecanismo de ação anti-hiperglicêmico dependente de glicose, os iDPP4 são particularmente adequados em pacientes com DRC. A maioria dos iDPP4 comumente prescritos (exceto linagliptina) são eliminados pelo rim, predominantemente inalterados como molécula-mãe (alogliptina, sitagliptina) ou como metabólitos (saxagliptina e vildagliptina). Consequentemente, os iDPP4 excretados por via renal são eliminados mais lentamente em pacientes com função renal reduzida e devem ser usados após ajuste da dose para que a exposição ao medicamento seja semelhante aos de pacientes com função renal normal21-23. A excreção renal possui um papel limitado na eliminação total da evogliptina e estudo farmacocinético e farmacodinâmico em pacientes portadores de DRC indicam que a evogliptina não demanda ajuste de dose renal para portadores de DRC leve a moderada18.
Vários iDPP4 vem sendo comercializados em todo o mundo nos últimos anos, constituindo uma classe terapêutica bastante conhecida e amplamente utilizada na abordagem terapêutica do DM2 em monoterapia (juntamente com dieta e exercícios físicos) ou em terapia combinada com outros agentes antidiabéticos21,23. No que diz respeito à segurança cardiovascular dos hipoglicemiantes orais, os iDPP4 em geral se mostraram seguros24. As evidências mais robustas de estudos cardiovasculares em larga escala (megatrials) não evidenciaram aumento de eventos cardiovasculares, incluindo mortalidade total ou por causa cardiovascular, ou de infarto do miocárdio não fatal e acidente vascular cerebral não fatal, associado ao uso de iDPP425-29. A segurança cardiovascular da evogliptina foi avaliada em estudo de vida real e os resultados confirmaram que o fármaco é no mínimo tão seguro quanto os demais representantes da classe dos iDPP4. Nesse estudo, os usuários de evogliptina apresentaram em relação aos usuários de glimepirida redução do risco de doença cardiovascular (aHR = 0,67; IC95% = 0,48 – 0,95; p = 0,025) e de eventos cerebrovasculares (aHR = 0,41; IC95% = 0,22 – 0,78; p = 0,007), não se observando associação significativa com a ocorrência de infarto agudo do miocárdio (aHR = 0,63; IC95% = 0,27 – 1,46; p = 0,282), insuficiência cardíaca (aHR = 0,35; IC95% = 0,09 – 1,47; p = 0,153), ataque isquêmico transitório (aHR = 0,23; IC95% = 0,03 – 1,72; p = 0,153) e angina pectoris (aHR = 1,35; IC95% = 0,82 – 2,21; p = 0,241)30.


1. Registro de medicamento novo, conforme RE 3.320 de 27/08/2021, publicado no DOU 164 de 30/08/2021. 2. Carr RD, Solomon A. Inhibitors of dipeptidyl peptidase-4 as therapeutic agents for individuals with type 2 diabetes: a 25-year journey. Diabet Med. 2020;37(8):1230–3. 3. Deacon CF, Nauck MA, Toft-Nielsen M, Pridal L, Willms B, Holst JJ. Both subcutaneously and intravenously administered glucagon-like peptide I are rapidly degraded from the NH2-terminus in type II diabetic patients and in healthy subjects. Diabetes. 1995;44(9):1126–31. 4. Dong-A ST – Suganon®. Disponível em: https://www.health.kr/searchDrug/result_drug.asp?drug_cd=2015100600006. Acesso em abril/2022. 5. Oh H, Nguyen HD, Yoon IM, Kim MS. Efficacy and Tolerability of Evogliptin in Patients with Type 2 Diabetes Mellitus: A Systematic Review and Meta-analysis with Bayesian Inference Through a Quality-management System. Clin Ther. 2021 Aug 1;43(8):1336–55. 6. Cercato C, Felício JS, Russo LAT, et al. Efficacy and safety of evogliptin in the treatment of type 2 diabetes mellitus in a Brazilian population: a randomized bridging study. Diabetol Metab Syndr. 2019 Dec 19;11:107. 7. Eurofarma. Suganon – bula do profissional de saúde. Disponível em: https://consultas.anvisa.gov.br/#/bulario/q/?nomeProduto=suganon. Acesso em abril/2022. 8. Gu N, Park MK, Kim TE, et al. Multiple-dose pharmacokinetics and pharmacodynamics of evogliptin (DA-1229), a novel dipeptidyl peptidase IV inhibitor, in healthy volunteers. Drug Des Devel Ther. 2014 Oct 6;8:1709-21. 9. Tan X, Hu J. Evogliptin: a new dipeptidyl peptidase inhibitor for the treatment of type 2 diabetes. Expert Opin Pharmacother. 2016 Jun;17(9):1285-93. 10. Kim G, Lim S, Kwon HS, et al. Efficacy and safety of evogliptin treatment in patients with type 2 diabetes: A multicentre, active-controlled, randomized, double-blind study with open-label extension (the EVERGREEN study). Diabetes Obes Metab. 2020 Sep;22(9):1527-1536. 11. Kim TE, Lim KS, Park MK, et al. Evaluation of the pharmacokinetics, food effect, pharmacodynamics, and tolerability of DA-1229, a dipeptidyl peptidase IV inhibitor, in healthy volunteers: first-in-human study. Clin Ther. 2012;34:1986-1998. 12. Kim MK, Chae YN, Kim HD, Yang EK, Cho EJ, Choi SH, et al. DA-1229, a novel and potent DPP4 inhibitor, improves insulin resistance and delays the onset of diabetes. Life Sci. 2012;90:21-9. 13. Kim HJ, Kwak WY, Min JP, Lee JY, Yoon TH, Kim HD, et al. Discovery of DA-1229: A potent, long acting dipeptidyl peptidase-4 inhibitor for the treatment of type 2 diabetes. Bioorg Med Chem Lett. 2011;21:3809-12. 14. Mulvihill, E. E. and Drucker, D. J. Pharmacology, physiology, and mechanisms of action of dipeptidyl peptidase-4 inhibitors. Endocr. Rev.2014 35, 992-1019. 15. Lankas GR, Leiting B, Roy RS, et al. Dipeptidyl peptidase IV inhibition for the treatment of type 2 diabetes: potential importance of selectivity over dipeptidyl peptidases 8 and 9. Diabetes. 2005 Oct;54(10):2988-94. 16. Nabeno M, Akahoshi F, Kishida H, et al. A comparative study of the binding modes of recently launched dipeptidyl peptidase IV inhibitors in the active site. Biochem Biophys Res Commun. 2013 May 3;434(2):191-6. 17. Filippatos TD, Athyros VG, Elisaf MS. The pharmacokinetic considerations and adverse effects of DPP-4 inhibitors [corrected]. Expert Opin Drug Metab Toxicol. 2014;10:787-812. 18. Oh J, Kim AH, Lee S, et al. Effects of renal impairment on the pharmacokinetics and pharmacodynamics of a novel dipeptidyl peptidase-4 inhibitor, evogliptin (DA-1229). Diabetes Obes Metab. 2017;19: 294-298. 19. Patel BD, Ghate MD. Recent approaches to medicinal chemistry and therapeutic potential of dipeptidyl peptidase-4 (DPP-4) inhibitors. Eur J Med Chem. 2014;74:1-32. 20. Thomas MC, Brownlee M, Susztak K, Sharma K, Jandeleit-Dahm KAM, Zoungas S, et al. Diabetic kidney disease. Nat Rev Dis Prim. 2015;1(October):1–20. 21. Davies MJ, D'Alessio DA, Fradkin J, et al. Management of Hyperglycemia in Type 2 Diabetes, 2018. A Consensus Report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2018 Dec;41(12):2669-2701. 22. Scheen AJ. Pharmacokinetics of dipeptidylpeptidase-4 inhibitors. Diabetes, Obesity and Metabolism 2010 12: 648–658. 23. Deacon CF. Dipeptidyl peptidase-4 inhibitors in the treatment of type 2 diabetes: a comparative review. Diabetes Obes Metab. 2011 Jan;13(1):7-18. 24. Scheen AJ. Cardiovascular effects of gliptins. Nat Rev Cardiol. 2013 Feb;10(2):73-84. 25. Scirica BM, Bhatt DL, Braunwald E, et al. Saxagliptin and cardiovascular outcomes in patients with type 2 diabetes mellitus. N Engl J Med. 2013 Oct 3;369(14):1317-26. 26. White WB, Cannon CP, Heller SR, et al. Alogliptin after acute coronary syndrome in patients with type 2 diabetes. N Engl J Med. 2013; 369:1327– 35. 27. Green JB, Bethel MA, Armstrong PW, Buse JB, Engel SS, Garg J, Josse R, Kaufman KD, Koglin J, Korn S, et al. Effect of sitagliptin on cardiovascular outcomes in type 2 diabetes. N Engl J Med. 2015;373(3):232–42. 28. Marx N, Rosenstock J, Kahn SE, et al. Design and baseline characteristics of the CARdiovascular outcome trial of LINAgliptin versus glimepiride in type 2 diabetes (CAROLINA®). Diab Vasc Dis Res. 2015;12:164–74. 29. Rosenstock J, Perkovic V, Johansen OE, et al. Effect of Linagliptin vs Placebo on Major Cardiovascular Events in Adults With Type 2 Diabetes and High Cardiovascular and Renal Risk: The CARMELINA Randomized Clinical Trial. JAMA. 2019 Jan 1;321(1):69-79. 30. Park SH, Jeong HE, Oh IS, et al. Cardiovascular safety of evogliptin in patients with type 2 diabetes: A nationwide cohort study. Diabetes Obes Metab. 2021 Jun;23(6):1232-1241.
ESTA TELA DESTINA-SE EXCLUSIVAMENTE A PROFISSIONAIS DE SAÚDE.
Este é um medicamento novo e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis para comercialização efeitos indesejáveis e não conhecidos podem ocorrer.